Blogs y actualizaciones
Nuestros blogs explican las afecciones de salud y la investigación clínica de una manera fácil de entender, para que los lectores se sientan más informados.
Los mejores servicios de ensayos clínicos para patrocinadores biotecnológicos: qué buscar y qué preguntar
Los patrocinadores de empresas biotecnológicas que buscan un socio para sus ensayos clínicos se enfrentan a un mercado muy saturado. Contar con el socio adecuado puede marcar la diferencia entre alcanzar los objetivos de reclutamiento a tiempo y ver cómo se retrasan los plazos. Esta guía detalla los aspectos que hay que tener en cuenta a la hora de seleccionar...
Los 6 criterios que definen una red de investigación clínica de primer nivel
No todas las redes de investigación clínica son iguales. Los patrocinadores y las organizaciones de investigación por contrato (CRO) que evalúan las redes de centros —así como los pacientes que buscan acceder a tratamientos de vanguardia— deben comprender qué distingue a una red de alto rendimiento de una red promedio. Este artículo analiza...
Trastornos endocrinos comunes y cómo tratarlos
Las hormonas son como mensajes de texto entre órganos, que permiten que las diferentes partes del cuerpo se comuniquen y se mantengan sincronizadas. Regulan el metabolismo, el estado de ánimo, la energía, el sueño e incluso el crecimiento. Son producidas por una red de glándulas llamada sistema endocrino y...
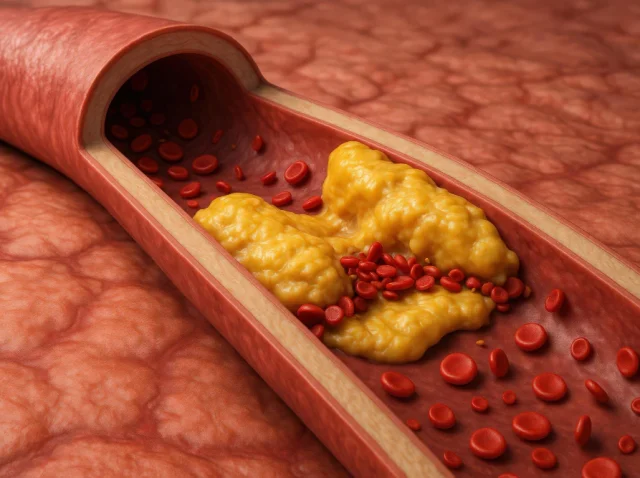
Por qué es importante realizarse pruebas periódicas para detectar la hipertrigliceridemia de manera temprana
Consideramos los análisis de sangre como algo rutinario, una parte estándar de los chequeos anuales que rara vez cuestionamos. Pero estas sencillas pruebas pueden revelar mucho sobre nuestra salud, a menudo antes de que aparezcan los síntomas. Uno de los hallazgos más silenciosos pero significativos que pueden...
Lo que nos enseñan las investigaciones recientes y los ensayos clínicos sobre la enfermedad tiroidea y su impacto en la salud.
Imagina una ciudad bulliciosa dentro de tu cuerpo, llena de billones de habitantes microscópicos que trabajan sin descanso. Así es la composición de tu microbioma intestinal, una compleja comunidad de microorganismos que viven en tu sistema digestivo. Estos diminutos residentes desempeñan un papel importante...
Un avance en la salud hepática supone una nueva esperanza para los ensayos clínicos y el tratamiento de las enfermedades del hígado.
Cuando pensamos en órganos vitales, puede que el hígado no sea el primero que nos viene a la mente. Sin embargo, en realidad desempeña un papel fundamental a la hora de mantenernos con vida. El hígado es responsable de procesar los nutrientes...
Los obstáculos y las promesas en los cánceres relacionados con el sistema endocrino
El cáncer es una enfermedad compleja y las investigaciones están cambiando constantemente nuestra comprensión de la misma. Una de las últimas novedades son los cánceres relacionados con el sistema endocrino (ERC), cánceres impulsados por las hormonas. El cáncer de mama y el de próstata han estado impulsados por las hormonas durante mucho tiempo, pero las investigaciones están demostrando que las hormonas pueden...
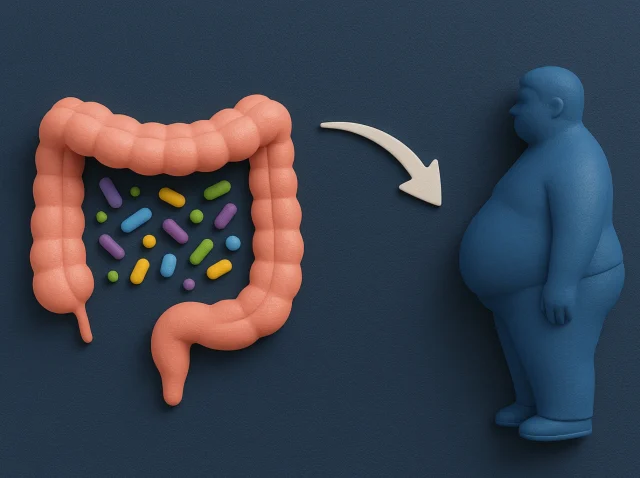
Tu intestino, tu salud: cómo los microbios del estómago influyen en el riesgo de padecer enfermedades metabólicas
La microbiota intestinal es una compleja comunidad de microorganismos que viven en el sistema digestivo. Estos microbios influyen en todo, desde la digestión hasta la función inmunitaria e incluso el control del peso. Profundicemos y veamos cómo la microbiota intestinal afecta a enfermedades metabólicas como la obesidad...
Por qué los niños necesitan estudios específicos sobre vacunación pediátrica
Los estudios sobre vacunación infantil constituyen la base de todo lo que sabemos sobre cómo proteger a los niños de enfermedades graves. Desde enfermedades comunes como la gripe hasta afecciones potencialmente mortales como la poliomielitis, se calcula que las vacunas salvan entre 2 y 3 millones de vidas al año en todo el mundo...
Avances en el tratamiento de los trastornos endocrinos
Tratamiento de los trastornos endocrinos: 5 avances significativos que están transformando la atención al paciente El tratamiento de los trastornos endocrinos está evolucionando rápidamente, ya que los avances en tecnología, medicina personalizada e investigación clínica abren nuevas vías para el manejo de las afecciones hormonales y metabólicas. El cuerpo humano depende del sistema endocrino...
Lo que los ensayos clínicos sobre hipertrigliceridemia nos enseñan sobre los medicamentos para reducir los triglicéridos
Ensayos clínicos sobre la hipertrigliceridemia: 6 hallazgos farmacológicos contrastados que marcan el rumbo del tratamiento Los ensayos clínicos sobre la hipertrigliceridemia están aportando a investigadores y médicos más información que nunca sobre cómo controlar los niveles elevados de triglicéridos y reducir los graves riesgos para la salud que estos conllevan. La hipertrigliceridemia se produce cuando los niveles de triglicéridos superan...
Cómo la medicina de precisión y los ensayos sobre obesidad están cambiando las opciones de tratamiento
Ensayos clínicos sobre la obesidad: 5 importantes avances en medicina de precisión que están transformando el tratamiento Los ensayos clínicos sobre la obesidad están a la vanguardia de una gran transformación en la forma en que entendemos y tratamos uno de los retos de salud pública más acuciantes del mundo. La obesidad está aumentando a nivel mundial a un ritmo de...